科研進展
西北高原所揭示母源性低氧暴露致雌性動物生殖損傷的改善策略
氧氣是動物生存的必要條件,其分壓變化對生殖發育具有關鍵調控作用。已有研究顯示,環境低氧可通過誘導代謝紊亂,影響母體妊娠過程,并對后代的器官發育及成年后健康產生持久影響。然而,胚胎期母源性低氧暴露對雌性生殖系統的長期作用機制,此前尚不明確。低氧暴露導致動物生殖損傷的干預策略研究也十分局限。
為系統解析胚胎期低氧對雌性生殖功能的調控網絡,中國科學院西北高原生物研究所動物生態與資源保護研究團隊構建了胚胎期(E0.5–E16.5)高原低氧暴露小鼠模型,探究環境低氧應激對雌性生殖功能的長期影響及其分子機制。結果發現,胚胎期低氧暴露的成年小鼠(4月齡)表現出生殖早衰表型,平均窩產仔數下降57.7%,卵巢儲備能力降低,各發育階段卵泡總數顯著減少。進一步研究表明,低氧組小鼠卵母細胞的成熟及發育潛能受損。研究團隊通過卵母細胞smart-seq測序和小鼠卵泡液代謝組分析,發現胚胎期低氧暴露下調Sirt3/Sod2信號通路,誘導線粒體功能紊亂,包括線粒體密度降低、膜電位下降和ATP生成減少,導致活性氧(ROS)過量積累與氧化應激加劇,進而引發卵母細胞DNA損傷和早期凋亡。此外,自噬相關基因表達下調,可能進一步加劇了卵母細胞損傷。卵泡與血清代謝組聯合分析顯示,低氧組小鼠煙酰胺單核苷酸(NMN)含量顯著降低,且NMN 代謝為核心差異富集通路。卵母細胞Sirt3過表達實驗驗證了該通路在低氧損傷修復中的關鍵作用。
基于上述機制,研究團隊開展了NMN干預實驗。結果顯示,連續14天體內注射NMN(200 mg/kg體重)顯著提高了低氧小鼠卵母細胞的成熟率與發育潛能,改善卵巢卵泡儲備;NMN處理組小鼠窩產仔數恢復至對照組的73.1%,后代胚胎發育能力顯著提升。本研究揭示了胚胎期低氧暴露對成年雌性生殖功能的潛在損傷,并表明補充煙酰胺單核苷酸(NMN)作為靶向干預手段,在改善低氧相關雌性生殖損傷中可能具有應用潛力。
相關研究成果以?Fetal hypoxia causes oocyte oxidative stress damage via Sirt3/sod2 pathway and could be alleviated by nicotinamide mononucleotide?為題,于2026年3月18日在線發表于 Zoological Research 雜志(中國科學院1區TOP期刊)。西北高原所博士后張璐瑤為論文第一作者,楊其恩研究員和中國農業大學侯云鵬副教授為通訊作者。該研究得到青海省自然基金團隊項目、國家自然科學基金及中國科學院特別研究助理等項目資助。
原文鏈接:https://www.zoores.ac.cn/article/doi/10.24272/j.issn.2095-8137.2025.579
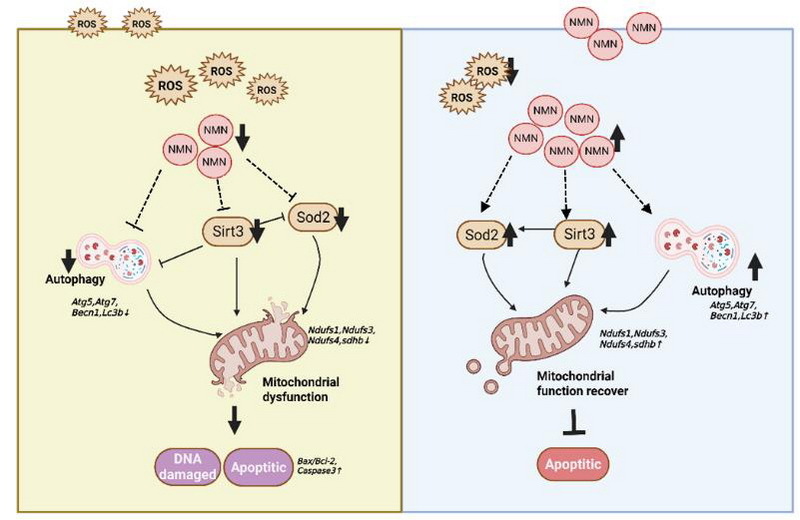
文章模式圖:胚胎期低氧通過 Sirt3/sod2 通路導致卵母細胞氧化應激損傷,而煙酰胺單核苷酸添加可以部分恢復卵母細胞及卵巢功能
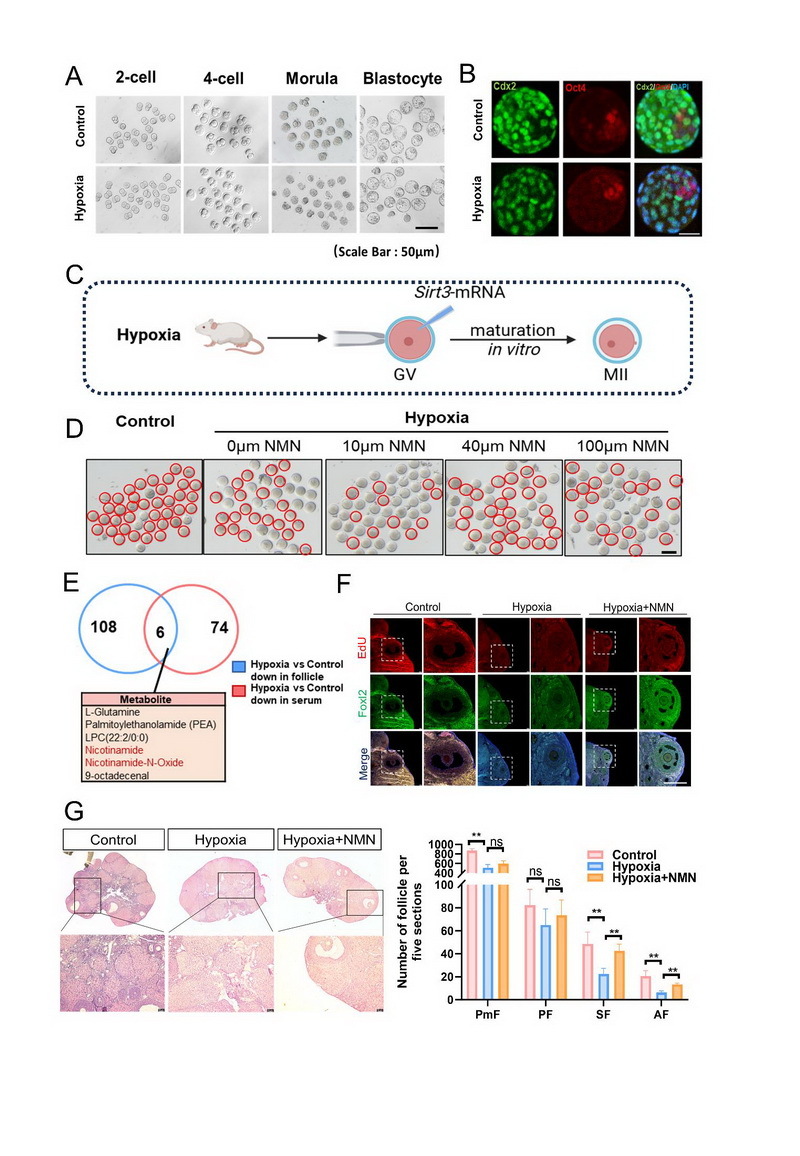
文章代表圖:(A)對照組與低氧組 2-細胞、4 -細胞、桑椹胚及囊胚期小鼠胚胎代表圖片(標尺:50 μm)。(B)對照組與低氧組囊胚中滋養層細胞標記物 Cdx2(綠色)、內細胞團標記物 Oct4(紅色)及核標記 DAPI(藍色)的免疫熒光共定位結果。(3)Sirt3 mRNA顯微注射低氧GV 期卵母細胞,進行Sirt3過表達實驗。 (D) 對照組及低氧組卵母細胞在不同濃度 NMN 體外處理后的成熟情況對比(紅色圈標記成熟卵母細胞,標尺:50 μm)。(E)低氧組與對照組卵泡液及血清中差異代謝物的交集分析,下方列出 6 個核心重疊差異代謝物。(F)對照組、低氧組及低氧 + NMN 組卵巢組織中增殖標記物 EdU(紅色)、顆粒細胞分化標記物 Foxl2(綠色)及 Merge 圖的免疫熒光結果(白色虛線框為局部放大區域,標尺:200 μm)。(G) 卵巢組織形態學分析與卵泡計數:對照組、低氧組及低氧 + NMN 組卵巢組織 H&E 染色結果(左圖,標尺為400 μm);各組原始卵泡(PmF)、初級卵泡(PF)、次級卵泡(SF)及有腔卵泡(AF)在 5 張連續切片中的數量統計(右圖)。








